Questões de Química - Físico-química - Termoquímica - Lei de Hess
TEXTO PARA A QUESTÃO.
Oxigênio (O2) e ozônio (O3) estão em constante processo de consumo e produção na estratosfera, como representado pelas equações químicas a seguir. As reações I e II ilustram etapas da produção de ozônio a partir de oxigênio, e a reação III mostra a restauração de oxigênio a partir de ozônio.

A reação global balanceada, composta pelas etapas I e II, que representa a formação de ozônio é:
Compressas de emergência quentes são usadas como primeiro socorro em contusões sofridas em práticas esportivas. Essa compressa constitui-se de um saco de plástico contendo uma ampola de água e um produto químico seco, por exemplo, o cloreto de cálcio (CaCℓ2). Com uma leve pancada, a ampola se quebra e o cloreto de cálcio se dissolve, conforme a reação representada pela equação:
CaCℓ2 (s) + H2O (ℓ) → CaCℓ2 (aq) ∆H = −82,7 kJ/mol
Nesse processo,
Dadas as equações termoquímicas, A e B, sendo
A) S(s) + O2(g) → SO2(g) ΔH = –297 kJ/mol
B) S(s) + 3/2 O2(g) → SO3(g) ΔH = –395 kJ/mol,
a variação de entalpia da seguinte reação SO3(g) → SO2(g) + ½ O2(g) é:
Na medicina veterinária, o cloreto de amônio (NH4Cl) é utilizado como acidulante da urina com o objetivo de evitar infecções. Para a produção do NH4Cl, é empregada a reação do ácido clorídrico (HCl) com amônia (NH3), representada abaixo:
HCl(aq) + NH3(aq) → NH4Cl(s) 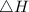 = ???
= ???
A partir dos valores das entalpias de formação do HCl ) , NH3
, NH3 ) e NH4Cl
e NH4Cl ) , determine a variação de entalpia
, determine a variação de entalpia ) da reação acima e se o processo é endotérmico ou exotérmico.
da reação acima e se o processo é endotérmico ou exotérmico.

A ilustração representa os caminhos alternativos para a conversão do ácido fórmico em monóxido de carbono e em dióxido de carbono.
Os caminhos alternativos representados na ilustração se fundamentam na
Observe a equação de formação de etanol a seguir:
2 Cgraf + 3 H2(g) + ½ O2(g) → C2H6O(l)
Com base nas equações abaixo que resultam na reação de interesse, calcule o ∆H da reação de formação do etanol.
I. Cgraf + O2(g) → CO2(g) ∆H = -394 kJ/mol
II. H2(g) + ½ O2(g) → H2O(l) ∆H = -286 kJ/mol
III. C2H6O(l) + 3 O2(g) → 2 CO2(g) + 3 H2O(l) ∆H = -1368 kJ/mol
Faça seu login GRÁTIS
Minhas Estatísticas Completas
Estude o conteúdo com a Duda
Estude com a Duda
Selecione um conteúdo para aprender mais:





