Resumo sobre Estequiometria - Química

Estequiometria
Passos para resolver:
- Montar a equação (reação)
- Balancear (caso não esteja balanceada)
- Identificar os envolvidos
- massa x massa
- volume x volume
- mol x massa
- etc
- Identificar a relação numérica (as quantidades)
- Montar a regra de três
- 1ª linha â†' valores padrão
- 2ª linha â†' dados pedidos
Grandezas envolvidas
- Massa atômica â†' u.m.a (u) é o número que está na tabela periódica
- Massa molecular â†' u.m.a (u) é a soma das massas atômicas
- Massa molar â†' grama/mol é numericamente igual à massa atômica
Volume molar â†' Litros
- Nas CNTP's â†' 1 mol = 22,4 L
- p = 1 atm
- T = 273 K (0°C)
- Fora das CNTP's â†' Equação dos Gases Ideais (Clapeyron)
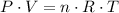
- P = pressão
- V = volume
- n = mols
- R = constante dos gases
- T = temperatura
Outros Casos
- Grau de Pureza (% massa)
- Limitante e Excesso (regra de três)
- Rendimento (% resultado)
Estude agora:



