A distribuição de velocidades das moléculas de um gás em um recipiente (um balão, por exemplo) obedece à chamada distribuição de Maxwell de velocidades (DMV). O gráfico a seguir mostra a DMV na situação em que três recipientes idênticos contêm um mesmo número de moléculas de oxigênio para as temperaturas de 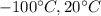 e
e 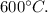 No gráfico, n(v) é o número de moléculas e 4 é a velocidade, em m/s. Nessa distribuição, a velocidade média das moléculas, a uma temperatura T, é
No gráfico, n(v) é o número de moléculas e 4 é a velocidade, em m/s. Nessa distribuição, a velocidade média das moléculas, a uma temperatura T, é %7D%2C) a velocidade mais provável de ser encontrada é
a velocidade mais provável de ser encontrada é 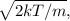 e a velocidade quadrática média é
e a velocidade quadrática média é 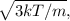 , em que K é a constante de Bolztmann e : é a massa das partículas.
, em que K é a constante de Bolztmann e : é a massa das partículas.

Tendo como referência as informações precedentes e considerando que o zero absoluto é 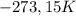 e que a constante dos gases é
e que a constante dos gases é 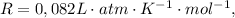 julgue o iten a seguir.
julgue o iten a seguir.
A DMV implica na possibilidade de violação de um ou mais princípios da Teoria da Relatividade Especial.





