Questões de Física - Termologia - Gases - Teoria cinética dos gases
Num experimento realizado no Laboratório de Física, um grupo de alunos observou que a pressão de uma amostra de gás, considerado ideal, era de 5,0 𝑎𝑡𝑚. A amostra passou por uma expansão isotérmica na qual o volume aumentou em 25%.
A partir dessas informações, podemos afirmar que o novo valor da pressão dessa amostra de gás ficou em:
Diversos processos na indústria de óleo e gás podem envolver misturas de gases a diferentes temperaturas. Um sistema isolado é composto por dois compartimentos de mesmo volume: o primeiro é ocupado por 𝑛ଵ = 1 mol e o segundo é ocupado por 𝑛2 = 2 mols de um gás ideal monoatômico. Inicialmente cada compartimento encontra-se em equilíbrio térmico, com temperatura 𝑇1 = 4𝑇 e 𝑇2 = 𝑇, respectivamente, conforme mostra a figura:

A partir de certo instante, a parede que separa os compartimentos é removida e, após algum tempo, o sistema atinge uma nova temperatura de equilíbrio 𝑇m.
Supondo que não há trabalho realizado após a remoção da parede, nem troca de calor entre o sistema e o ambiente externo, a temperatura de equilíbrio 𝑇m é dada por:

A distribuição de velocidades das moléculas de um gás em um recipiente (um balão, por exemplo) obedece à chamada distribuição de Maxwell de velocidades (DMV). O gráfico a seguir mostra a DMV na situação em que três recipientes idênticos contêm um mesmo número de moléculas de oxigênio para as temperaturas de 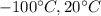 e
e 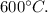 No gráfico, n(v) é o número de moléculas e 4 é a velocidade, em m/s. Nessa distribuição, a velocidade média das moléculas, a uma temperatura T, é
No gráfico, n(v) é o número de moléculas e 4 é a velocidade, em m/s. Nessa distribuição, a velocidade média das moléculas, a uma temperatura T, é %7D%2C) a velocidade mais provável de ser encontrada é
a velocidade mais provável de ser encontrada é 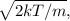 e a velocidade quadrática média é
e a velocidade quadrática média é 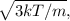 , em que K é a constante de Bolztmann e : é a massa das partículas.
, em que K é a constante de Bolztmann e : é a massa das partículas.

Tendo como referência as informações precedentes e considerando que o zero absoluto é 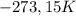 e que a constante dos gases é
e que a constante dos gases é 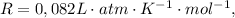 julgue o iten a seguir.
julgue o iten a seguir.
As três curvas apresentadas no gráfico têm a mesma área.
O físico italiano Enrico Fermi, baseado nos estudos da expansão adiabática na atmosfera, propôs que, a cada 0,5 km que subimos em altitude, a temperatura ambiente se reduz em 5 K.
Dessa forma, se inicialmente estivermos num local a 800 m de altitude, em relação ao nível do mar e a uma temperatura ambiente de 25 ºC, ao descermos para uma cidade a 200 m do nível do mar, a temperatura estará em torno de
Para encher o pneu de sua bicicleta, um ciclista, conforme figura a seguir, dispõe de uma bomba em formato cilíndrico, cuja área de seção transversal (A) é igual a 20 cm2 . A mangueira de conexão (M) é indeformável e tem volume desprezível.

O pneu dianteiro da bicicleta tem volume de 2,4 L e possui, inicialmente, uma pressão interna de 0,3 atm. A pressão interna da bomba, quando o êmbolo (E) está todo puxado à altura (H) de 36 cm, é igual a 1 atm (pressão atmosférica normal).
Considere que, durante a calibragem, o volume do pneu permanece constante e que o processo é isotérmico, com temperatura ambiente de 27 ºC.
Nessas condições, para elevar a pressão do pneu até 6,3 atm, o número de repetições que o ciclista deverá fazer, movendo o êmbolo até o final do seu curso, é
Na figura abaixo, EH2 e EO2 e VH2 e VO2 são, respectivamente, as energias cinéticas médias e as velocidades médias das moléculas de uma amostra de gás H2 e de outra, de gás O2, ambas em temperatura de 27 ºC.

Assinale a alternativa que relaciona corretamente os valores das energias cinéticas médias e das velocidades médias das moléculas de H2 e de O2.
Faça seu login GRÁTIS
Minhas Estatísticas Completas
Estude o conteúdo com a Duda
Estude com a Duda
Selecione um conteúdo para aprender mais:




